VCE化学 | Unit3 AOS1最强复习笔记
转眼,12年级的Term1 已经结束,Unit 3 AOS 1,也就是VCE化学的第一个AOS 1 的复习也将开始了。今天老师就来带大家详细梳理一番!
这部分的内容主要可以分为Fuel和Cell两个模块:~fuel相关~Obtaining energy from fuelsFuel choices~cell相关~Galvanic cells as a source of energyFuel cells as a source of energy两者又通过fuel cell 联系在一起。
下面这篇文章主要目的是为大家分析一下整个AOS1重点考察的知识点,以及每个知识点通常涉及的考察方式和题型。
VCE化学AOS1|第一部分:Obtaining energy from fuels

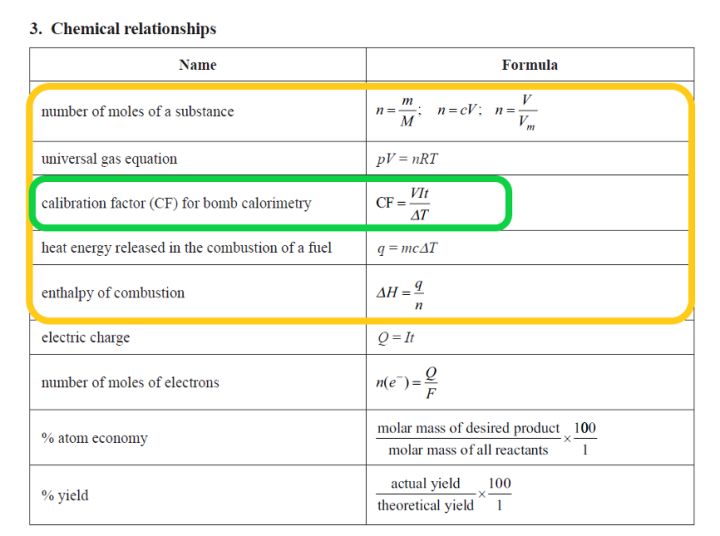
考点一:Calculation (计算题)为主。
从data booklet可以看到,VCE化学考试中考察的计算主要包括Stoichiometry, gas equation,energy/enthalpy,Faraday‘s law 和 yield. 其中加粗的三项(即黄框中的内容)都属于Unit 3 AOS 1。(绿框中的CF公式是q=mcΔT在bomb calorimetry中的延伸,在Heinemann Chemistry Chapter 17。一些学校会选择与AOS 1一起考察,也有一些会选择留到Y12最后。)
这部分中的计算题也很可能在一道题中结合多个知识点,例如 determine the net volume of greenhouse gases at a given temperature and pressure (pV=nRT) released per MJ of energy obtained (ΔH=q/n & stoichiometry)。
考点二:Complete / Incomplete combustion reaction of alkane / alcohol (写equation的题,涉及stoichiometry)
1.complete combustion produce H2O & CO2(g)
2.incomplete combustion produce H2O + CO(g) or H2O + C(s) (两种incomplete combustion取决于燃烧时的氧含量,题目中通常会注明product 是 CO 还是C)
考点三:Writing thermochemical equations (equation+ΔH,涉及stoichiometry)
1. ΔH的单位是kJ/mol ,即kJ per mol reaction 而非per mol reactant。要注意equation 中的coefficient并据此计算ΔH。
2. 对于exothermic reaction,外界温度上升,q=mcΔT算得的energy 为positive,但ΔH此时为negative。Endothermic则反之。因此一定要注意正负号的问题。
VCE化学AOS1|第二部分 Fuel choice
考点一:Explanation & justification (简答题) 为主。
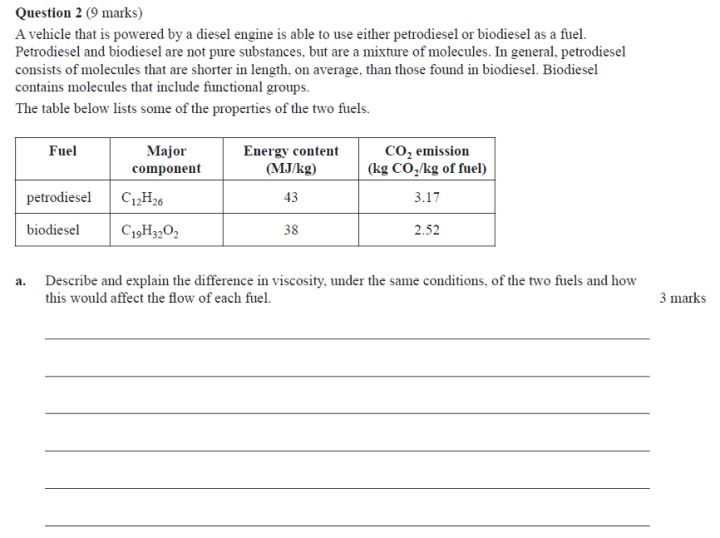
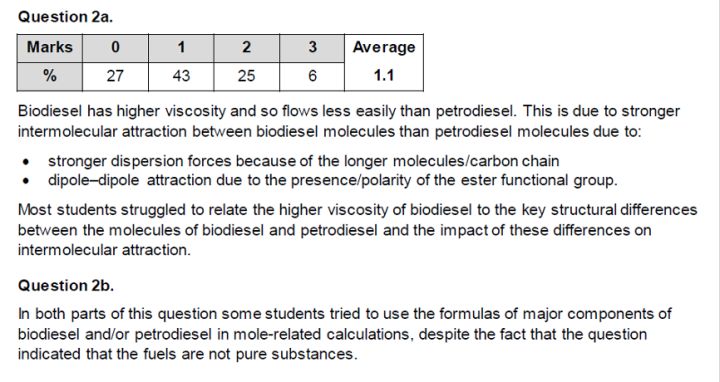
主要在于比较fossil fuel 与biofuel。一个重点是通过intermolecular forces 比较physical properties (viscosity, cloud point, hygroscopic property) ofbiodiesel and petroldiesel ,由此也可以分析其应用,例如低温下应使用petroldiesel而非biodiesel。另一个重点是讨论environmental impact of fuels。
考点二:reactions related to fuel production (写equation / 分析reaction)
1. Photosynthesis (produce glucose, related to bioethanol)
2. Anaerobic respiration (fermentation) of yeast (production of bioethanol)
3. transesterification (production of biodiesel, 与triglyceride相关的condensation/ hydrolysis将在Unit 4 AOS 2进一步讨论)
例题 VCE 化学2017 Question 2
VCE化学AOS1|第三、第四部分:Galvanic cells & fuel cell


这两个部分主要的题型是Cell图分析题。考点通常是比较系统化的,涉及的重点有:
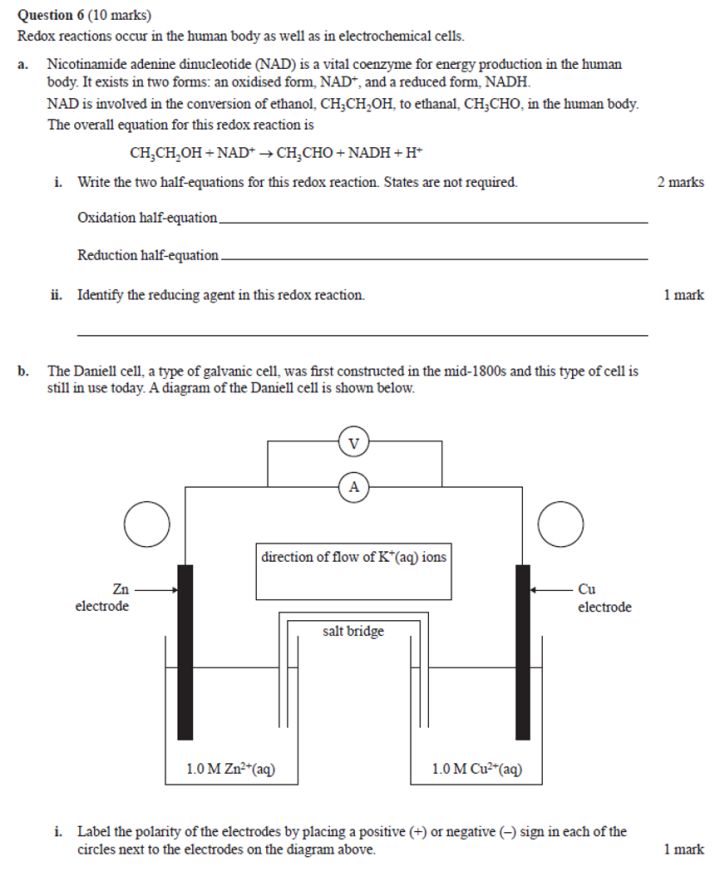
➮Writing/balancing half-equation & overall ionic equation of redox reaction (写equation的题)
➮Analysing design features & chemical processes of cell(在图中标注,或低分的简答题):
| 1.identify anode & cathode2.identify positive & negative electrode (请注意*anode – at which oxidation reaction occur 与negative electrode 是不同的概念,也不总是在同一个electrode。这一点在AOS 2 electrolysis 中会深入讨论) 3.function of electrode, electrolyte, salt bridge, membrane4.use of porous electrodes for gaseous reactant (mostly in fuel cells)5.direction of electron flow6.direction of ions flow |
➮Comparing concepts(高分的简答题):
1.Exothermic redox reaction & galvanic cell
2.Combustion of fuel & fuel cell
3.Primary cell,secondary cell & fuel cell
➮Use of electrochemical series (变体较多的简答题,可能延展为分析题,例如分析the result of changing the material of a specific electrode):
1.predicting products of reaction
2.deducing overall redox reaction
3.determine maximum voltage (under SLC, 1M concentration)
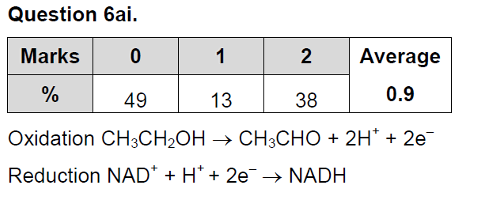
例题 VCE 化学2018 Question 6

答案




结 语
相信大家看完以上的内容,一定对Unit 3 AOS 1的复习有了更深的了解。接下来希望大家能够通过对方法的实践取得自己满意的成绩。如果大家想要了解更多针对ACE化学的复习,快速解决以上问题,也欢迎联系我们,为你的VCE化学保驾护航!
END
添加龙老师
预约VCE化学在线试听
获取私人定制学习计划












